Plano define grupos prioritários que serão vacinados contra a covid no 1º semestre de 2021
- Detalhes
- Categoria: Saúde
- Publicado: Terça, 24 Novembro 2020 18:16
- Escrito por Redação
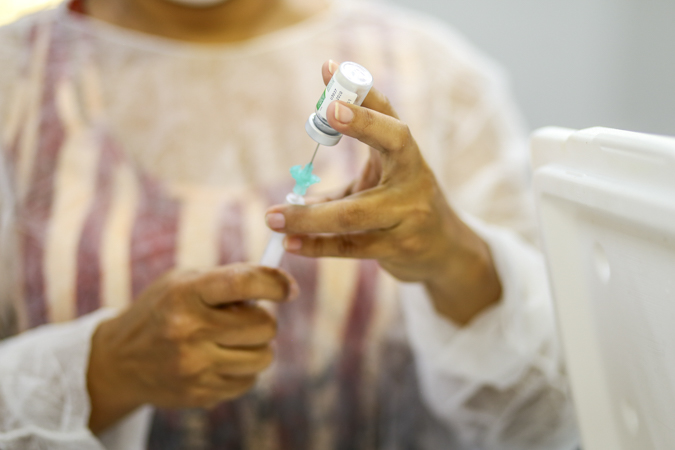 O Governo do Piauí informou nesta terça-feira (24) que está elaborando um plano de logística para a vacinação contra a Covid-19. Diversos setores da Secretaria de Saúde do Estado (Sesapi) estão envolvidos na estratégia que, de acordo com o governo, pretende ser iniciada ainda no primeiro semestre de 2021, a depender da liberação da vacina.
O Governo do Piauí informou nesta terça-feira (24) que está elaborando um plano de logística para a vacinação contra a Covid-19. Diversos setores da Secretaria de Saúde do Estado (Sesapi) estão envolvidos na estratégia que, de acordo com o governo, pretende ser iniciada ainda no primeiro semestre de 2021, a depender da liberação da vacina.
Segundo o plano, que ainda está em elaboração, os grupos prioritários na primeira fase de vacinação seriam os idosos acima de 80 anos, pessoas com comorbidades e profissionais da saúde. A Sesapi e os municípios farão um trabalho de busca a este público.
“Esse processo de imunização vai demandar uma grande estrutura da Sesapi, por isso estamos nos planejando com antecedência para que possamos realizar com êxito todo o processo da imunização Covid-19. Esse é um planejamento que requer muito cuidado e demandará um esforço ainda maior de todos os setores da secretaria”, afirma o secretário de Estado da Saúde, Florentino Neto.
Segundo a Sesapi, o planejamento já está sendo estudado há mais de 40 dias em parceria com o Ministério da Saúde, pelos setores que vão da Atenção Básica, Alta Complexidade em Saúde, Vigilância Sanitária e Comunicação, como explica a diretora de Vigilância e Atenção em Saúde da Sesapi, Cristiane Moura Fé.
“Todo o procedimento de distribuição e organização da rede ficará a cargo da Coordenação de Imunização da Sesapi, através das 11 Regionais de Saúde. Por isso estamos fazendo um levantamento de nossa capacidade instalada, para podermos fazer essa megaoperação a contento, já que teremos uma demanda diferente das demais vacinações, onde chamamos à população e desta vez será ela que virá nos acionar para que seja vacinada. Por isso a mobilização de todos os setores”, afirma.
Cristiane Moura Fé destaca que no primeiro momento não haverá vacina para toda a população.
“No primeiro momento infelizmente não teremos vacina para toda população do estado. Dessa forma as pessoas serão estratificadas em grupos prioritários, e esse trabalho a Sesapi fará em consonância com os municípios, para que tenhamos celeridade no cumprimento desta missão. A expectativa do Ministério da Saúde é que no primeiro semestre de 2021 se vacine os grupos prioritários, que corresponde a mais ou menos 50% da população, e no segundo semestre os demais”, destaca a diretora.
Entre as estratégias que estão sendo montadas pela Sesapi está a preparação da rede de distribuição de imunobiológicos e a operacionalização das salas de vacinas nos municípios. Atualmente, não há vacinas disponíveis contra a Covid-19. No Brasil receberam autorização para experimentos de larga escala no as vacinas desenvolvidas pelos laboratórios AstraZeneca/Oxford, Sinovac, Janssen e Pfizer/Biontech/Fosun Pharma.
“Temos uma perspectiva, por enquanto, de três tipos de vacinas a serem disponibilizadas a esses grupos. Duas delas, teremos que administrá-la em duas doses, que é algo diferenciado e precisará de uma logística especial em dois momentos. Por isso estamos iniciando esta preparação para que no momento em que as vacinas sejam liberadas, nossa rede esteja toda estruturada para suprir a demanda”, enfatiza Cristiane Moura Fé.










































 A Organização Mundial da Saúde (OMS) anunciou nesta segunda-feira, 23, que a "aposta mais segura" para algumas famílias será não realizar reuniões familiares neste Natal e ano-novo para impedir a disseminação do coronavírus. Festas de Ano Novo, com aglomeração, também não são recomendadas.
A Organização Mundial da Saúde (OMS) anunciou nesta segunda-feira, 23, que a "aposta mais segura" para algumas famílias será não realizar reuniões familiares neste Natal e ano-novo para impedir a disseminação do coronavírus. Festas de Ano Novo, com aglomeração, também não são recomendadas.
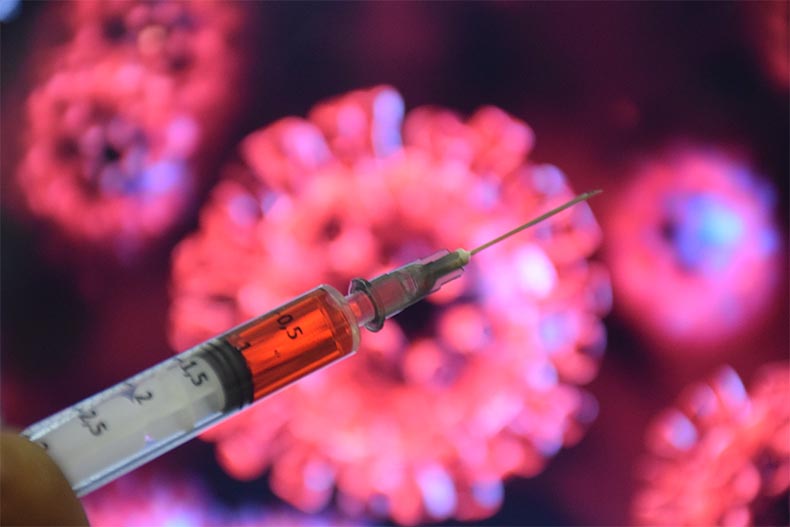 A vacina contra a Covid-19 da Universidade de Oxford (Reino Unido) produzida em parceria com a farmacêutica AstraZeneca atingiu eficácia de até 90%, segundo análise dos resultados preliminares de ensaio clínico de fase 3.
A vacina contra a Covid-19 da Universidade de Oxford (Reino Unido) produzida em parceria com a farmacêutica AstraZeneca atingiu eficácia de até 90%, segundo análise dos resultados preliminares de ensaio clínico de fase 3. O governador Wellington Dias (PT) revelou durante uma live na manhã desta segunda-feira (23) que os governadores estão otimistas que a vacina da Covid-19 deverá ser disponibilizada ainda em janeiro de 2021. Wellington Dias, que representa todos os governadores do País na articulação pró-vacina, disse que a primeira vacina que for aprovada pelos órgãos de saúde deverá ser disponibilizada à população.
O governador Wellington Dias (PT) revelou durante uma live na manhã desta segunda-feira (23) que os governadores estão otimistas que a vacina da Covid-19 deverá ser disponibilizada ainda em janeiro de 2021. Wellington Dias, que representa todos os governadores do País na articulação pró-vacina, disse que a primeira vacina que for aprovada pelos órgãos de saúde deverá ser disponibilizada à população.